

NO1 激光在美国的管制情况
FDA是美国食品药品监督管理局的简称,监管美国食品、医疗、激光、化妆品产品在美国销售的许可和监督。凡是含有激光的产品出口到美国,因为其存在激光辐射隐患,均受FDA管制,由CDRH部门负责具体监管和准入事宜。比如激光医疗器械、激光美容仪、激光机械、消费类激光产品、激光玩具、工矿用激光、激光舞台、激光测量探测等等均为管制对象。

NO2 FDA认证流程
2.1关于检测
2.1.1 检测确认:
a,提供产品规格书,确认检测费用;
b,确认费用,双方签合同;
c,邮寄样品,开始安排测试;d,出具检测报告草稿,确认信息;
e,报告确认OK,出报告正式盖章档。
注:
1,咨询费用时,需要提供激光产品规格书、电路图、产品图片等资料;
2,检测周期一般1-2周,需要根据具体产品而定,整改周期不算在内;
2.1.2 测试标准
FDA激光可以直接使用21CFR 1040.10+21CFR 1040.11(指示器、舞台灯、医疗激光适用)或, IEC 60825-1+Laser Notice 56.
2.1.3
连续激光测试流程如下
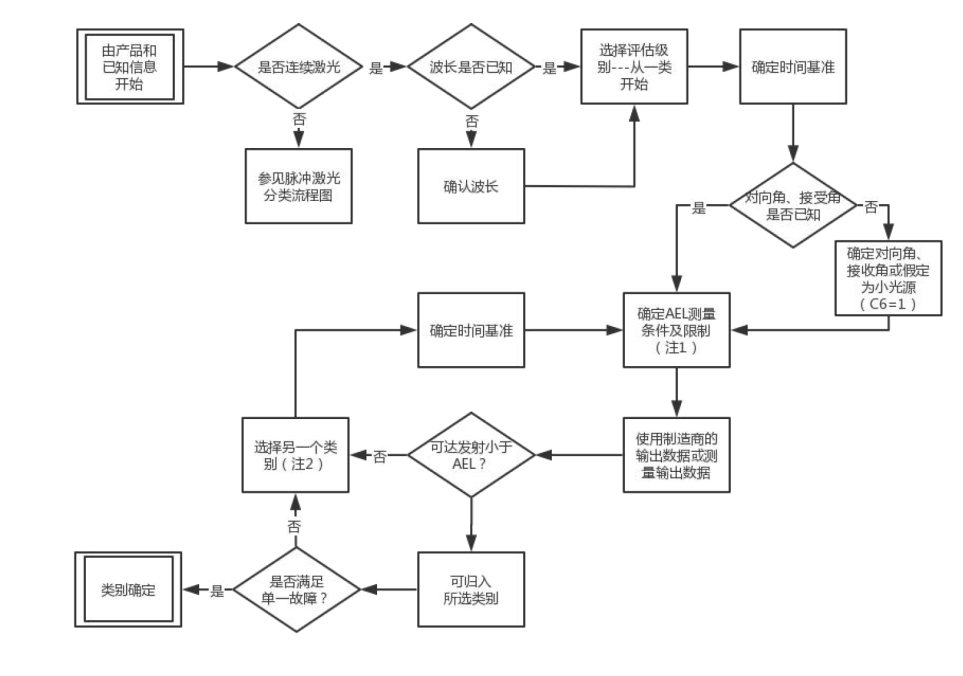
脉冲激光测试流程如下
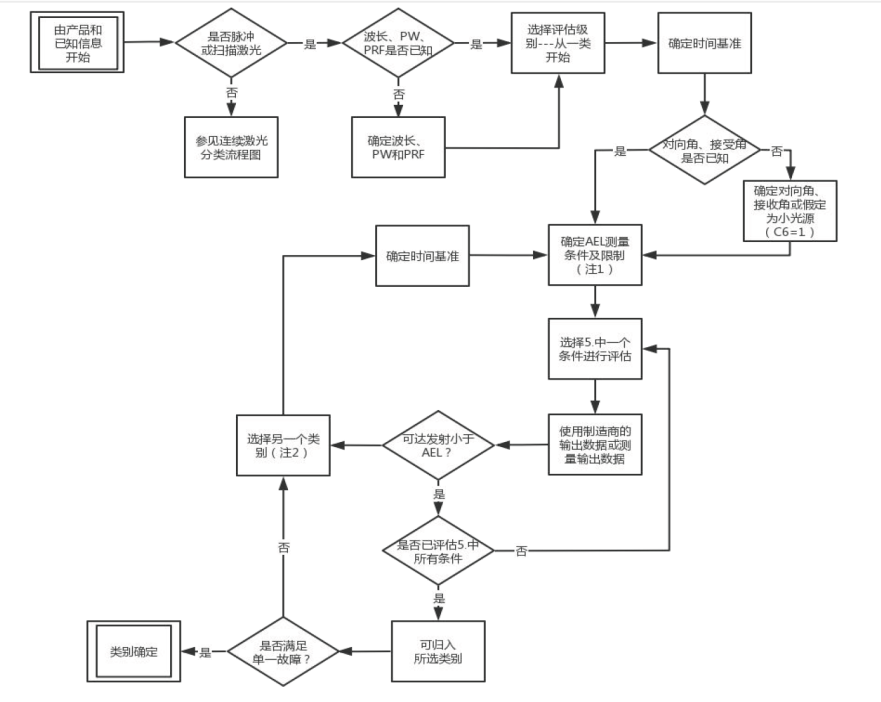
2.1.3 激光标记
21 CFR 1040.10激光标签如下
等级 | 标签 |
Class I | 无要求 |
Class IIa (标识文字即可) | Class IIa Laser Product - Avoid Long-Term Viewing of Direct Laser Radiation. |
Class II |
|
Class IIIa (<2.5mw/cm2 用黄色) (>2.5mw/cm2 用红色) |
|
Class IIIb |
|
Class IV |
|
IEC 60825-1激光标签如下
等级 | 标签 |
Class 1 |
|
Class 1M |
|
Class 1C |
|
Class 2 |
|
Class 2M |
|
Class 3R |
|
Class 3B |
|
Class 4 |
|
2.1.4 认证标记
测试合格后,需要在产品上贴认证标记(此处认证标签更多是声明的意思,而不是认证机构颁发的认证标志),如下
直接使用21CFR 1040.10+21CFR 1040.11进行测试的 | 使用IEC 60825-1+Notice 56进行测试的 |
Complies with 21 CFR 1040.10 and 1040.11 | Complies with FDA performance standards for laser products except for conformance with IEC 60825-1 Ed. 3., as described in Laser Notice No. 56, dated May 8, 2019. |
另,均需增加制造商名称、地址和生产日期 | |

2.2 关于注册:
注册为常规大众接受的称谓,FDA称之为报告。
依据规则分为:
首次报告:21 CFR 1002.10
补充报告:21CFR 1002.11(如适用)
简化报告:21CFR 1002.12(部分产品适用)
年度报告:21CFR 1002.13(每年9.1至10.1间进行)
意外辐射事故报告:21CFR 1002.20(如有发生)
检测合格后进行首次报告,完成后获得FDA档案回执(含Accession Number)。
报告资料含量大部分
第一部分,产品技术资料,包括但不限于:激光检测报告、产品规格书、电路图、光路图、结构图、产品铭牌、激光标签、认证标签、产品标识照等
第二部分,生产过程质量保证资料,包括但不限于:出厂QC检验报告(含激光功率监控和其他关键项目)、测试仪器校准报告、寿命及可靠性测试方案和记录、生产流程关键步骤、关键器件清单和质量保证程序、美国代理人协议、产品质量声明等。
同时,制造商还应依据21CFR 1002.30做好生产制造记录,依据21CFR 1002.31做好产品检查测试记录。
NO3 关于产品出口

--FDA注册后,是没有证书的,FDA官方是不会出任何证书;如果有证书,均是第三方服务机构自己出的,与FDA无关;
--FDA logo 不允许运用到任何报告或证书上,也不允许打印到产品或外包装上;但是注册号码可以打印到产品和包装上;
--FDA注册后,次年开始的每一年都需要进行年报(如上21CFR 1002.13);
--FDA注册,以制造商公司为主体的进行注册。
--进口激光产品到美国时,进口商需要宣告进口的电子产品需要符合美国法规要求。即需要填报FORM FDA 2877表。内容要素有:进口港口、进口编号、制造商名称地址和原产国、进口商的名称地址、产品描述(名称)、产品数量、型号和商标、及注册是获得的Accession Number。
--特别警告:
根据《美国法典》第18编第1001条,任何人故意作出虚假申报,可被处以不超过10000美元的罚款或不超过5年的监禁,或两者并罚。
任何人进口不符合要求的电子产品也可能会受到1000美元-300000美元的罚款。

返回顶部